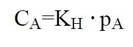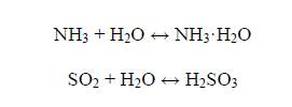gaasid vees
Sisevetes sisalduvate gaaside peamiseks allikaks on otseselt või kaudselt atmosfäär. Atmosfääri moodustab pika aja jooksul stabiliseerunud koostisega gaaside segu (tabel 1).
Tabel 1. Peamised atmosfääris leiduvad gaasid.
Tabel 1. Peamised atmosfääris leiduvad gaasid.
Gaas |
Molekulmass |
Suhteline sisaldus ruumalas, % |
N2 |
28,013 |
78,084 |
O2 |
31,998 |
20,948 |
Ar |
29,948 |
0,934 |
CO2 |
44,010 |
0,04 |
Ne |
20,183 |
0,00182 |
He |
4,003 |
0,00524 |
CH4 |
16,043 |
0,00017 |
Atmosfääri praegune koostis on väga erinev esialgse ürgse atmosfääri omast ja selliseks on see kujunenud peamiselt elusorganismide toimel. Taolise gaasisegu üheks esmaseks iseloomustajaks on keskmine molekulmass. See on segu koostises olevate gaaside molekulmasside kaalutud keskmine ja selle väärtus on 28,9645. Atmosfääri suhtelist koostist väljendatakse kas massi või ruumala järgi. Vastavalt siis, millise osa iga gaas moodustab kas õhu ühikulisest massist või ühikulisest ruumalast. Põhigaasideks on lämmastik ja hapnik. Teisi gaase esineb õhus tunduvalt väiksemates kogustes. Kui veel suhteliselt ohtra sisaldusega argoon juurde arvata, siis on tublisti üle 99,9 % kuiva õhu ruumalast täidetud. Ülejäänud gaase nimetatakse viimasel lisandgaasideks, kuid nende roll pole sellest hoolimata vähemtähtis nii atmos- kui ka hüdrosfääris.
Kõik nimetatud gaasid on vees lahustuvad ja veemassi gaasikoostise tasakaal atmosfääriga saavutatav. Atmosfääris leiduvad gaasid lahustuvad vees siiski võrdlemisi halvasti (va CO2). Pinnaveekogud on harilikult küllastunud lämmastiku, argooni ja lisandgaasidega, kuid hapniku ja süsihappegaasi sisaldus varieerub vee-elustiku tõttu. Lahustunud hapnik on veekvaliteedi seisukohalt oluline, kuna seda vajatakse hingamisel ja veesamba ning sette-vee piirpinna aeroobse keskkonna säilitamiseks. Süsihappegaas on fotosünteesi süsinikuallikaks ja looduvete pH määrajaks. Lahustunud lämmastiku on võrreldes teiste gaasidega rohkem, kuid selle mõju bioloogilistele ja keemilistele protsessidele on tunduvalt väiksem kui hapnikul võis süsihappegaasil. Ülejäänud gaasidel on veekvaliteedile väike mõju.
Vees lahustunud gaaside hulk sõltub võrdlemisi paljudest teguritest, mis on erinevad näiteks mineraalainete lahustumisega võrreldes. Esiteks sõltub gaasi lahustuvus gaasi molekulaarsetest omadustest. Loodusvetes leiduvate gaaside lahustuvus pole ühesugune tänu erinevale molekulaarsele iseloomule ja seda iseloomustatakse konkreetse gaasi adsorbtsioonikoefitsendiga. Näiteks CO2 lahustub vees palju paremini kui CH4. Teiseks oluliseks teguriks on temperatuur. Reeglina soodustab kõrgem temperatuur ainete lahustumist, kuid gaaside lahustuvus on vastavalt Le Chatelier´ printsiibile pöördvõrdeline temperatuuriga. Näiteks N2 lahustuvus tema normaalse osarõhu korral on 0 ºC juures 23,04 mg/l, aga 30 ºC juures vaid 12,58 mg/l. Kolmandaks lahustuvust määravaks teguriks on soolsus. Soolade sisalduse kasvades väheneb gaaside lahustuvus. Seda tuleb arvestada näiteks soolajärvede gaasisisalduse hindamisel, kus lahustunud gaaside kogused on alati väiksemad võrreldes mageveega. Ja neljandaks sõltub gaaside lahustuvus rõhust. Rõhu suurenedes kasvab ka gaaside lahustuvus ja rõhk on üks peamistest loodusvete gaasikoostist reguleerivatest teguritest. Konstantsel temperatuuril toimub gaaside lahustumine nende osarõhu alusel, mida väljendab Henry seadus:
Kõik nimetatud gaasid on vees lahustuvad ja veemassi gaasikoostise tasakaal atmosfääriga saavutatav. Atmosfääris leiduvad gaasid lahustuvad vees siiski võrdlemisi halvasti (va CO2). Pinnaveekogud on harilikult küllastunud lämmastiku, argooni ja lisandgaasidega, kuid hapniku ja süsihappegaasi sisaldus varieerub vee-elustiku tõttu. Lahustunud hapnik on veekvaliteedi seisukohalt oluline, kuna seda vajatakse hingamisel ja veesamba ning sette-vee piirpinna aeroobse keskkonna säilitamiseks. Süsihappegaas on fotosünteesi süsinikuallikaks ja looduvete pH määrajaks. Lahustunud lämmastiku on võrreldes teiste gaasidega rohkem, kuid selle mõju bioloogilistele ja keemilistele protsessidele on tunduvalt väiksem kui hapnikul võis süsihappegaasil. Ülejäänud gaasidel on veekvaliteedile väike mõju.
Vees lahustunud gaaside hulk sõltub võrdlemisi paljudest teguritest, mis on erinevad näiteks mineraalainete lahustumisega võrreldes. Esiteks sõltub gaasi lahustuvus gaasi molekulaarsetest omadustest. Loodusvetes leiduvate gaaside lahustuvus pole ühesugune tänu erinevale molekulaarsele iseloomule ja seda iseloomustatakse konkreetse gaasi adsorbtsioonikoefitsendiga. Näiteks CO2 lahustub vees palju paremini kui CH4. Teiseks oluliseks teguriks on temperatuur. Reeglina soodustab kõrgem temperatuur ainete lahustumist, kuid gaaside lahustuvus on vastavalt Le Chatelier´ printsiibile pöördvõrdeline temperatuuriga. Näiteks N2 lahustuvus tema normaalse osarõhu korral on 0 ºC juures 23,04 mg/l, aga 30 ºC juures vaid 12,58 mg/l. Kolmandaks lahustuvust määravaks teguriks on soolsus. Soolade sisalduse kasvades väheneb gaaside lahustuvus. Seda tuleb arvestada näiteks soolajärvede gaasisisalduse hindamisel, kus lahustunud gaaside kogused on alati väiksemad võrreldes mageveega. Ja neljandaks sõltub gaaside lahustuvus rõhust. Rõhu suurenedes kasvab ka gaaside lahustuvus ja rõhk on üks peamistest loodusvete gaasikoostist reguleerivatest teguritest. Konstantsel temperatuuril toimub gaaside lahustumine nende osarõhu alusel, mida väljendab Henry seadus:
kus, CA on gaasi A kontsentratsioon lahuses (mol/l; mg/l) ja pA gaasi A osarõhk lahuse kohal (atm). Et gaaside lahustuvus pole ühesuguse osarõhu korral võrdne, tuleb iga gaasi puhul kasutada antud gaasile temperatuurist sõltuvat konstanti ehk Henry konstanti (KH ; (mol·l)/atm; (mg·l)/atm).
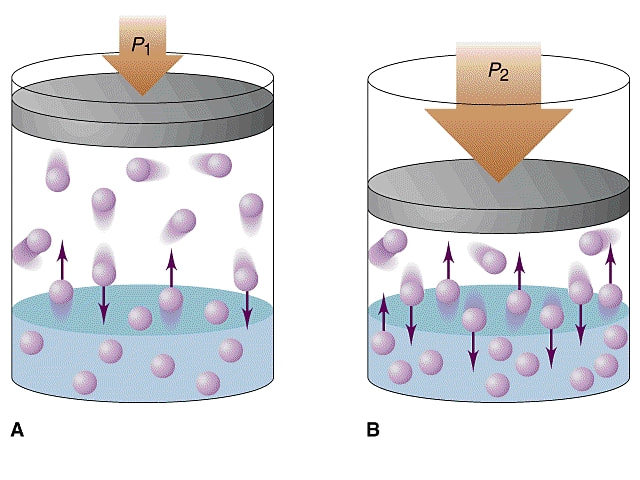
Henry seaduse põhjal on gaasi lahustuvus vedelikus proportsionaalne selle osarõhuga lahuse kohal (joonis 1).
Henry seaduse põhjal on gaasi lahustuvus vedelikus proportsionaalne selle osarõhuga lahuse kohal (joonis 1).
Osarõhk ehk partsiaalrõhk on rõhk, mida mingi gaasisegu komponent avaldaks, kui see vaadeldav komponent esineks üksi samal temperatuuril ja samal ruumalal. Osarõhkude seaduse kohaselt on üksteisega mittereageerivate ideaalsete gaaside segu kogurõhk võrdne segu moodustavate gaaside osarõhkude summaga. Gaasisegu (nt õhu) iga koostisosa lahustuvus on proportsionaalne antud gaasi osarõhuga lahuse kohal olevas gaasisegus.
Rõhu kiire vähenemine põhjustab osa gaasi eraldumist lahusest mullidena. Taoline olukord tekib näiteks gaseeritud joogi pudeli kiirel avamisel ning põhjustab kessoontõbe akvalangistidel. Henry seadus ei kehti siiski gaaside puhul, mis osaliselt veega reageerivad ja annavad oodatust parema lahustuvuse.: